Введение
В исследовании EORTC 1333 «PEACE-3» изучалась комбинация энзалутамида и 6 ежемесячных инъекций радия-223 (Ra223) у пациентов с метастатическим кастрационно-резистентным раком предстательной железы (мКРРПЖ) и метастазами в кости.
Материалы и методы
С ноября 2015 по март 2023 года 446 пациентов, включая 11, получавших абиратерон, были рандомизированы на группы, получавшие энзалутамид (без плацебо) или энзалутамид в сочетании с шестью циклами Ra223. С марта 2018 года было обязательным одновременное применение золедроновой кислоты или деносумаба. Первичной конечной точкой была выживаемость без радиологического прогрессирования заболевания (рВБП) по оценке исследователя. Ключевые вторичные конечные точки включали общую выживаемость (ОВ), время до последующего системного лечения, прогрессирование боли и симптоматические скелетные осложнения.
Результаты
Отношение рисков (ОР) для рВБП составило 0,69 [95% доверительный интервал (ДИ) 0,54–0,87, P = 0,0009], при этом медиана rPFS составила 16,4 месяца (95% ДИ 13,8–19,2 месяца) в группе энзалутамида и 19,4 месяца (95% ДИ 17,1–25,3 месяца) в группе комбинированной терапии. При запланированном промежуточном анализе, проведенном при 80% случаев общей выживаемости (ОВ), ОР для ОВ составило 0,69 (95% ДИ 0,52–0,90, P = 0,0031), при этом медиана ОВ составила 35,0 месяцев (95% ДИ 28,8–38,9 месяца) в группе энзалутамида и 42,3 месяца (95% ДИ 36,8–49,1 месяца) в группе комбинированной терапии. В связи с непропорциональным риском это будет дополнительно проверено при окончательном анализе общей выживаемости. Нежелательные явления, возникшие в ходе лечения (НЯ) ≥ 3 степени тяжести, были зарегистрированы у 55,8% и 65,6% пациентов в группах энзалутамида и комбинированной терапии соответственно. Наиболее частыми НЯ ≥ 3 степени тяжести в группе комбинированной терапии были гипертензия (34%), усталость (6%), перелом (5%), анемия (5%) и нейтропения (5%). Переломы, как возникшие в ходе лечения, так и после лечения, симптоматические или патологические, с применением или без применения костно-защитных средств (КЗС) были зарегистрированы у 30 (13,4%) пациентов в группе энзалутамида и у 53 пациентов (24,3%) в группе комбинированной терапии.
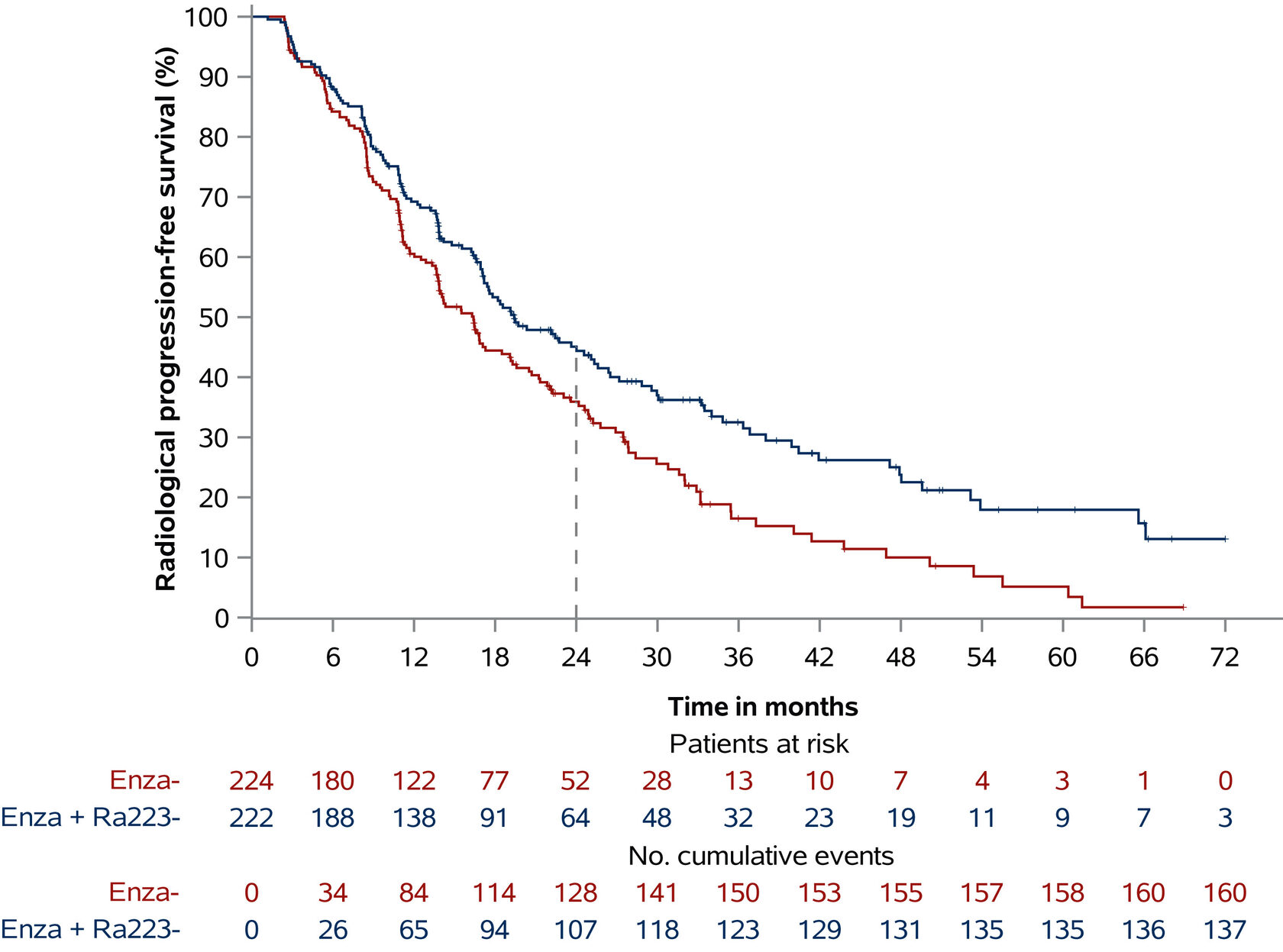
Выживаемость без радиологического прогрессирования, оценённая местным исследователем в популяции ITT. Отношение рисков (ОР) и 95% доверительный интервал (95% ДИ) для всех пациентов рассчитаны с использованием модели пропорциональных рисков Кокса, стратифицированной по исходному болевому синдрому, предшествующему применению доцетаксела и использованию костно-протекторных препаратов на момент рандомизации.
Enza — энзалутамид; ITT — анализ по принципу «намерение лечить»; Ra-223 — радий-223.
Enza — энзалутамид; ITT — анализ по принципу «намерение лечить»; Ra-223 — радий-223.
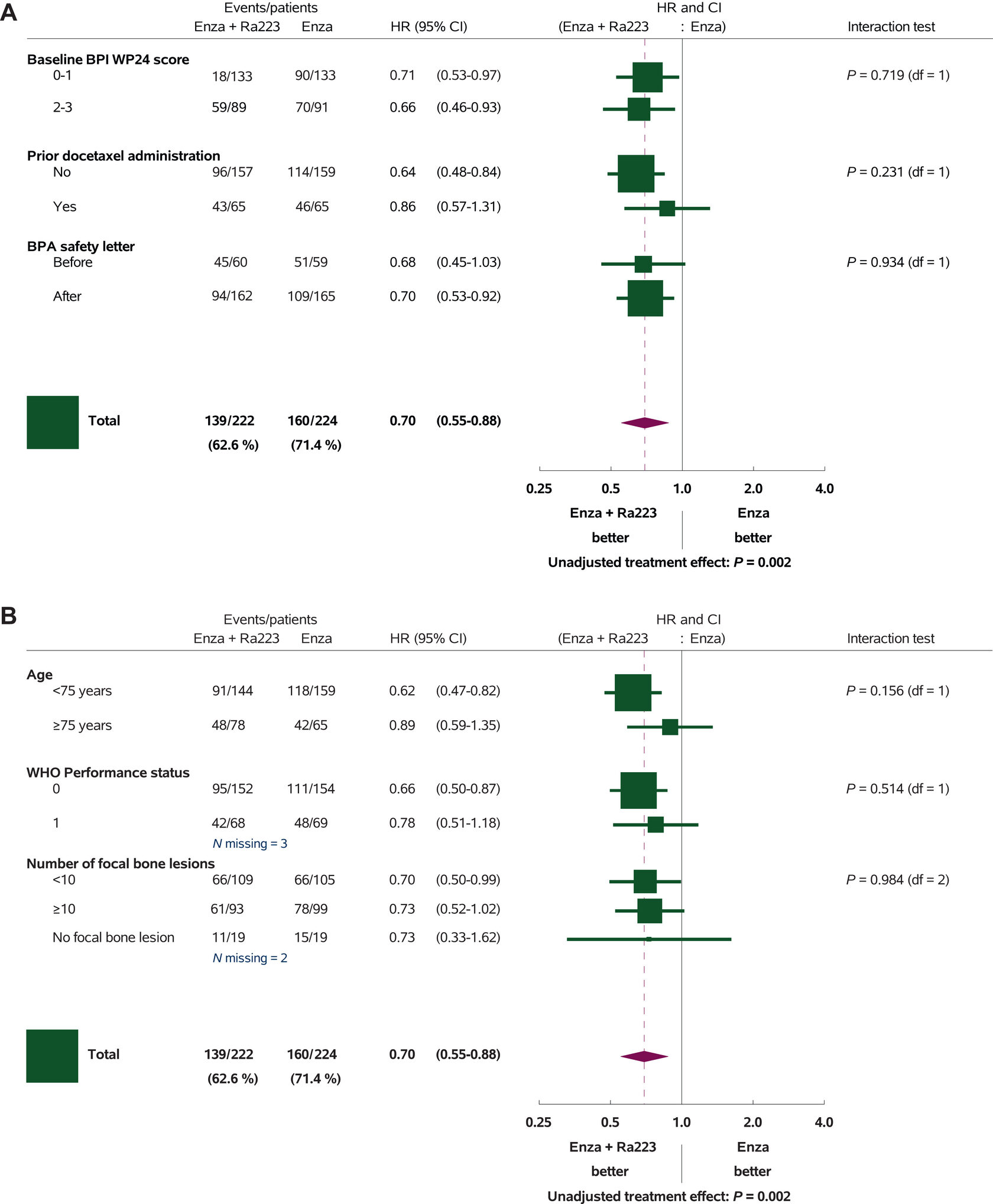
Рисунок 2. Анализ подгрупп выживаемости без радиологического прогрессирования, оценённый местным исследователем.
(A) Анализ с учётом факторов стратификации, использованных при рандомизации.
(B) Анализ дополнительных клинически значимых подгрупп. Эффект лечения в данном анализе не стратифицирован, поэтому он не отражает основной анализ исследования и рассматривается как анализ чувствительности.
BPA — костно-защитный агент; CI — доверительный интервал; Enza — энзалутамид; HR — отношение рисков; Ra-223 — радий-223.
(A) Анализ с учётом факторов стратификации, использованных при рандомизации.
(B) Анализ дополнительных клинически значимых подгрупп. Эффект лечения в данном анализе не стратифицирован, поэтому он не отражает основной анализ исследования и рассматривается как анализ чувствительности.
BPA — костно-защитный агент; CI — доверительный интервал; Enza — энзалутамид; HR — отношение рисков; Ra-223 — радий-223.
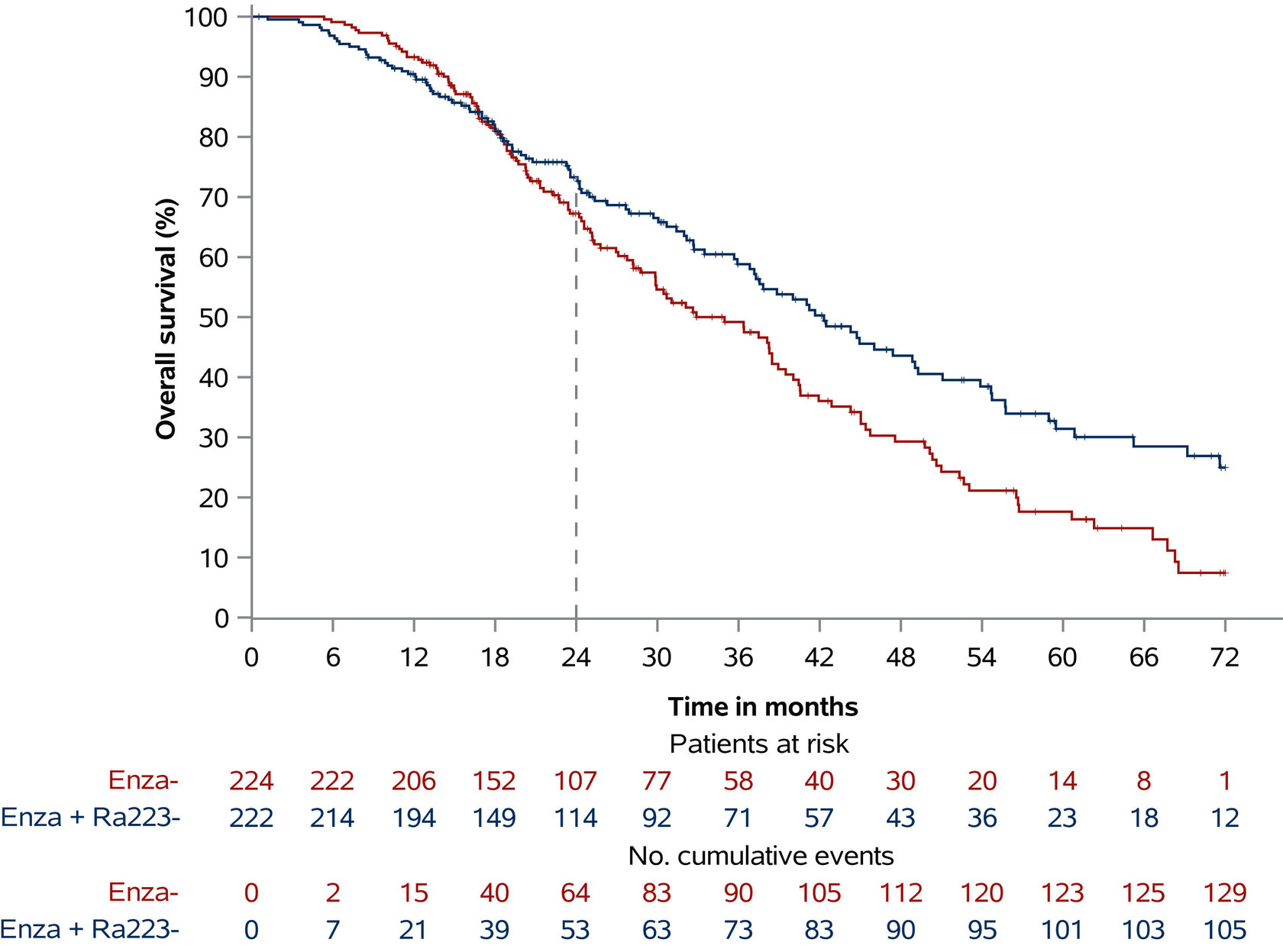
Рисунок 3. Общая выживаемость в популяции ITT. Отношение рисков (ОР) и 95% доверительный интервал (95% ДИ) для всех пациентов рассчитаны с использованием модели пропорциональных рисков Кокса, стратифицированной по исходному болевому синдрому, предшествующему применению доцетаксела и использованию костно-защитного препарата на момент рандомизации.
Enza — энзалутамид; ITT — анализ по принципу «намерение лечить»; Ra-223 — радий-223.
Enza — энзалутамид; ITT — анализ по принципу «намерение лечить»; Ra-223 — радий-223.
Заключение
Исследование PEACE-3 демонстрирует, что сочетание энзалутамида с Ra223 в качестве терапии первой линии при метастатическом раке предстательной железы значительно улучшает выживаемость без прогрессирования заболевания. Хотя результаты статистически значимы на промежуточном этапе оценки общей выживаемости, исследование будет продолжено до окончательного анализа общей выживаемости.
