ВВЕДЕНИЕ
С внедрением комбинаций на основе ингибиторов контрольных точек (ИКТ) в первую линию терапии метастатического почечно-клеточного рака (мПКР) остро встал вопрос выбора оптимальной второй линии лечения. Несмотря на широкое использование кабозантиниба, проспективные данные о его применении именно во 2-й линии после ИКТ-комбинаций до настоящего времени были ограничены.
МЕТОДЫ И МАТЕРИАЛЫ
CaboPoint — проспективное многоцентровое исследование II фазы, в котором оценивалась эффективность и безопасность кабозантиниба во 2-й линии терапии у пациентов с мПКР после прогрессирования на первой линии ИКТ-комбинаций.
В исследование включено 127 пациентов, распределённых на две когорты:
– после комбинации ниволумаб + ипилимумаб (ИКТ–ИКТ)
– после комбинации ИКТ + VEGF-ТКИ
Первичной конечной точкой была частота объективного ответа (ЧОО) по данным независимой центральной оценки. Вторичные конечные точки включали выживаемость без прогрессирования (ВБП), общую выживаемость (ОВ) и безопасность.
В исследование включено 127 пациентов, распределённых на две когорты:
– после комбинации ниволумаб + ипилимумаб (ИКТ–ИКТ)
– после комбинации ИКТ + VEGF-ТКИ
Первичной конечной точкой была частота объективного ответа (ЧОО) по данным независимой центральной оценки. Вторичные конечные точки включали выживаемость без прогрессирования (ВБП), общую выживаемость (ОВ) и безопасность.
РЕЗУЛЬТАТЫ
Медиана наблюдения составила 19,3 месяца.
Частота объективного ответа:
– 40,5% — после ИКТ–ИКТ
– 27,5% — после ИКТ + VEGF-ТКИ
По оценке исследователей ЧОО достигала 49,4% и 33,3% соответственно.
Медиана выживаемости без прогрессирования:
– 10,9 месяца — после ИКТ–ИКТ
– 8,3 месяца — после ИКТ + VEGF-ТКИ
Медиана общей выживаемости была сопоставима между группами и составила около 24 месяцев.
Контроль заболевания превышал 80% в обеих когортах.
Профиль безопасности соответствовал ранее известным данным. Нежелательные явления 3–4 степени наблюдались у 75,6% пациентов, наиболее часто — артериальная гипертензия, диарея и тромбоэмболические осложнения. Новых сигналов токсичности не выявлено.
Частота объективного ответа:
– 40,5% — после ИКТ–ИКТ
– 27,5% — после ИКТ + VEGF-ТКИ
По оценке исследователей ЧОО достигала 49,4% и 33,3% соответственно.
Медиана выживаемости без прогрессирования:
– 10,9 месяца — после ИКТ–ИКТ
– 8,3 месяца — после ИКТ + VEGF-ТКИ
Медиана общей выживаемости была сопоставима между группами и составила около 24 месяцев.
Контроль заболевания превышал 80% в обеих когортах.
Профиль безопасности соответствовал ранее известным данным. Нежелательные явления 3–4 степени наблюдались у 75,6% пациентов, наиболее часто — артериальная гипертензия, диарея и тромбоэмболические осложнения. Новых сигналов токсичности не выявлено.
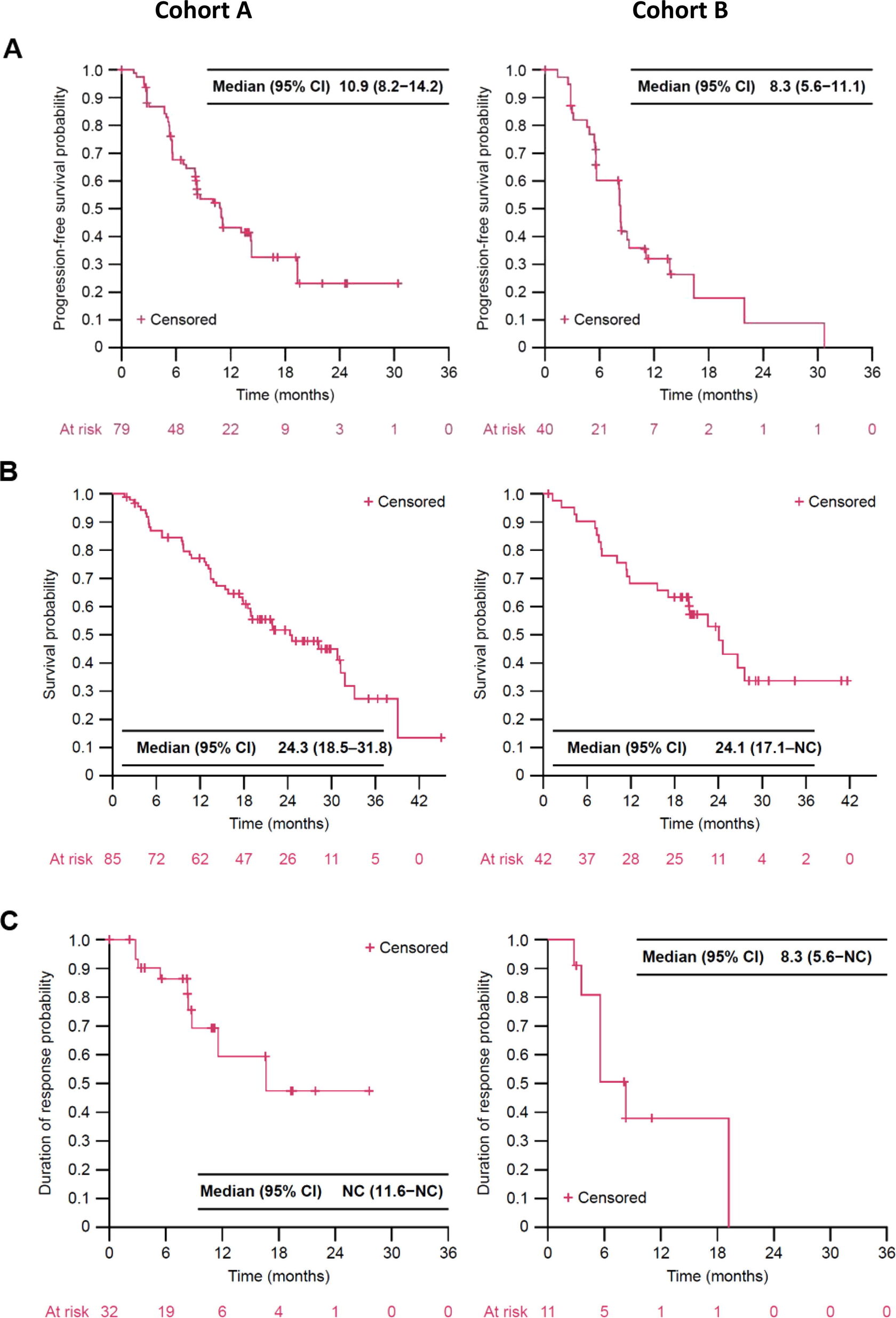
(A) Выживаемость без прогрессирования (ВБП) по данным независимой центральной оценки (ICR), (B) общая выживаемость (ОВ) и (C) длительность ответа (DOR) по данным ICR в когорте A (предшествующая CPI–CPI терапия) и когорте B (предшествующая CPI + VEGF-таргетная терапия).
Анализ ВБП и DOR по ICR: n = 119 (когорта A — 79, когорта B — 40). DOR анализировалась только у пациентов с ответом (32/79 в когорте A и 11/40 в когорте B).
Анализ ОВ: n = 127 (когорта A — 85, когорта B — 42).
ВБП определялась как время от начала лечения до прогрессирования заболевания или смерти от любой причины. ОВ — как время от начала лечения до смерти. DOR — как время от первого зафиксированного ответа до прогрессирования или смерти.
ВБП и DOR цензурировались на момент последней оценки опухоли у пациентов без прогрессирования или смерти на момент отсечки данных.
Пациенты цензурировались:
(1) при начале несоответствующей протоколу противоопухолевой терапии — на дату последней оценки до её начала;
(2) при отсутствии события к моменту отсечки данных — на дату последней оценки;
(3) при наступлении события после пропуска ≥2 плановых оценок — на дату последней оценки.
В общей популяции медиана ВБП составила 9,0 месяца (95% ДИ 8,2–11,1), медиана ОВ — 24,3 месяца (95% ДИ 19,2–30,8).
CI — доверительный интервал; CPI — ингибиторы контрольных точек; DOR — длительность ответа; ICR — независимая центральная оценка; NC — не вычисляется; OS — общая выживаемость; PFS — выживаемость без прогрессирования; VEGF — сосудистый эндотелиальный фактор роста.
Анализ ВБП и DOR по ICR: n = 119 (когорта A — 79, когорта B — 40). DOR анализировалась только у пациентов с ответом (32/79 в когорте A и 11/40 в когорте B).
Анализ ОВ: n = 127 (когорта A — 85, когорта B — 42).
ВБП определялась как время от начала лечения до прогрессирования заболевания или смерти от любой причины. ОВ — как время от начала лечения до смерти. DOR — как время от первого зафиксированного ответа до прогрессирования или смерти.
ВБП и DOR цензурировались на момент последней оценки опухоли у пациентов без прогрессирования или смерти на момент отсечки данных.
Пациенты цензурировались:
(1) при начале несоответствующей протоколу противоопухолевой терапии — на дату последней оценки до её начала;
(2) при отсутствии события к моменту отсечки данных — на дату последней оценки;
(3) при наступлении события после пропуска ≥2 плановых оценок — на дату последней оценки.
В общей популяции медиана ВБП составила 9,0 месяца (95% ДИ 8,2–11,1), медиана ОВ — 24,3 месяца (95% ДИ 19,2–30,8).
CI — доверительный интервал; CPI — ингибиторы контрольных точек; DOR — длительность ответа; ICR — независимая центральная оценка; NC — не вычисляется; OS — общая выживаемость; PFS — выживаемость без прогрессирования; VEGF — сосудистый эндотелиальный фактор роста.
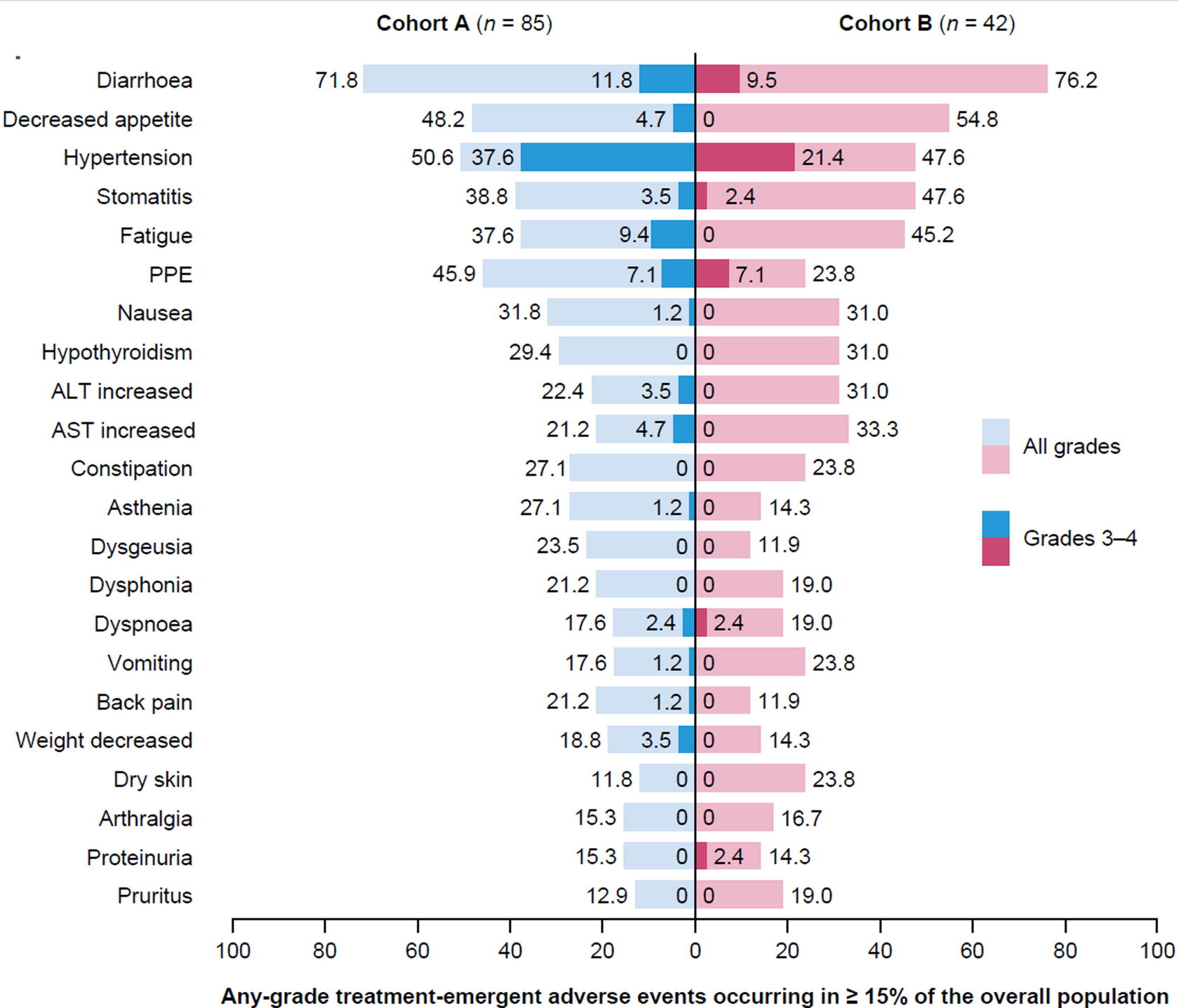
Наиболее частые нежелательные явления, возникшие на фоне лечения, по степени тяжести (популяция безопасности; N = 127).
ALT — аланинаминотрансфераза; AST — аспартатаминотрансфераза; PPE — ладонно-подошвенная эритродизестезия; TEAE — нежелательное явление, возникшее на фоне лечения.
ALT — аланинаминотрансфераза; AST — аспартатаминотрансфераза; PPE — ладонно-подошвенная эритродизестезия; TEAE — нежелательное явление, возникшее на фоне лечения.

Частота объективного ответа (ORR) и контроля заболевания (DCR) по (A) независимой центральной оценке (ICR; n = 119) и (B) оценке исследователя (n = 127) в когорте A (предшествующая CPI–CPI терапия) и когорте B (предшествующая CPI + VEGF-таргетная терапия).
ORR определяется как доля пациентов с полным или частичным ответом. DCR — как доля пациентов с полным ответом, частичным ответом или стабилизацией заболевания.
Проценты ORR и DCR рассчитаны от общего числа пациентов с доступными данными; пациенты с отсутствующими данными считались неответившими. Проценты BOR (лучший общий ответ) рассчитывались на основании пациентов с доступными данными; пациенты с отсутствующими данными не включались в анализ ICR и LIR.
BOR — лучший общий ответ; CI — доверительный интервал; CPI — ингибиторы контрольных точек; DCR — контроль заболевания; ICR — независимая центральная оценка; LIR — оценка исследователя; ORR — объективный ответ; VEGF — сосудистый эндотелиальный фактор роста.
a Восемь пациентов (шесть в когорте A и два в когорте B) были исключены из первичного анализа эффективности из-за отсутствия исходных измеряемых очагов для центральной оценки.
b Сравнение с порогом 10% (по данным исследования METEOR) выполнено с использованием точного биномиального теста (одновыборочного).
ORR определяется как доля пациентов с полным или частичным ответом. DCR — как доля пациентов с полным ответом, частичным ответом или стабилизацией заболевания.
Проценты ORR и DCR рассчитаны от общего числа пациентов с доступными данными; пациенты с отсутствующими данными считались неответившими. Проценты BOR (лучший общий ответ) рассчитывались на основании пациентов с доступными данными; пациенты с отсутствующими данными не включались в анализ ICR и LIR.
BOR — лучший общий ответ; CI — доверительный интервал; CPI — ингибиторы контрольных точек; DCR — контроль заболевания; ICR — независимая центральная оценка; LIR — оценка исследователя; ORR — объективный ответ; VEGF — сосудистый эндотелиальный фактор роста.
a Восемь пациентов (шесть в когорте A и два в когорте B) были исключены из первичного анализа эффективности из-за отсутствия исходных измеряемых очагов для центральной оценки.
b Сравнение с порогом 10% (по данным исследования METEOR) выполнено с использованием точного биномиального теста (одновыборочного).
ЗАКЛЮЧЕНИЕ
Исследование CaboPoint впервые проспективно демонстрирует эффективность кабозантиниба во 2-й линии терапии после современных ИКТ-комбинаций при мПКР. Полученные результаты подтверждают его клиническую активность и поддерживают использование в качестве стандартной опции после прогрессирования на иммунотерапии.
В то же время отсутствие рандомизированного сравнения и ограниченный объём выборки не позволяют окончательно определить место кабозантиниба среди других стратегий второй линии, что требует дальнейших исследований.
В то же время отсутствие рандомизированного сравнения и ограниченный объём выборки не позволяют окончательно определить место кабозантиниба среди других стратегий второй линии, что требует дальнейших исследований.